台灣第2家國產疫苗廠聯亞生技,昨天進行二期臨床試驗期中分析報告,結果顯示安全性和耐受性都良好,所有受試者未出現疫苗相關嚴重不良反應,粗估保護力達80到90%,同時在6月底送件至食藥署,申請EUA緊急使用授權,通過後盼儘快供民眾施打。
聯亞生技昨天晚間宣布,武漢肺炎疫苗二期臨床試驗期中分析結果,發言人范瀛云表示,「分析結果顯示安全性與耐受性良好,所有受試者未出現嚴重不良反應,並規劃在今年11月中下旬,進行試驗解盲。
范瀛云表示,於變異株有效保護力的部分,UB612誘導出的中和性抗體,對印度delta株的效價,仍保持同一個水平並強調,自家疫苗「可以對抗Delta突變株」。聯亞抗體效價在施打第二劑後28天血清陽轉率,於19至64歲施打疫苗組達95.65%、65歲以上年長者施打疫苗組則達88.57%;中和抗體效價為102.3。
另一間國產疫苗高端也於6/10宣布解盲成功,不但安全性良好,沒有嚴重不良反應;全年齡血清陽轉率99.8%,幾乎全部受試者都誘發免疫記憶;中和抗體效價溝更高達662,GMT倍率比值163倍,而表現在20到60歲之間的族群效果更好,幾乎全部會誘發免疫反應,並產生中和抗體。
高端採用雙盲測試,讓受試者和研究者,兩邊都不知道誰打疫苗、誰打安慰劑,避免影響到研究者的判斷,從不良反應副作用來看,7成的人出現注射部位疼痛,疲倦、頭痛、發燒等輕微副作用,顯示安全性也夠。
至於中和抗體效價,就是「產生能對抗病毒抗體的濃度」,數值「越高越好」。高端達662,聯亞針對65歲以上為102.3,AZ為372;莫德納為373,高端在中和抗體效價數據比聯亞高。
但食藥署署長吳秀梅提醒,來自不同實驗室,難以做比較。聯亞2期期中報告分析後就能先送件食藥署,並進一步規畫審查EUA期程。
(民視新聞網/綜合報導)
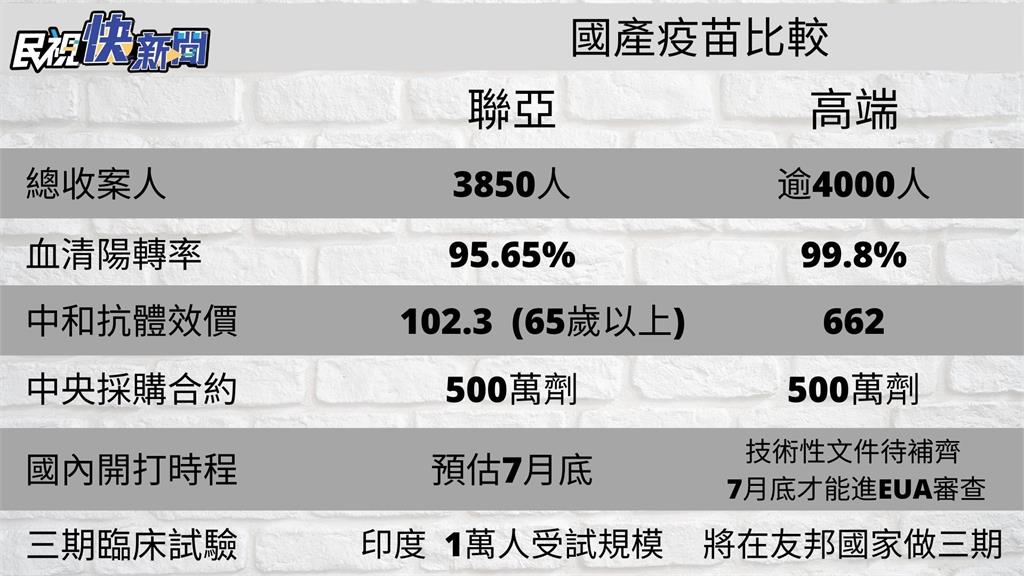 高端聯亞比較圖(圖/民視新聞)
高端聯亞比較圖(圖/民視新聞)
更多新聞: 快新聞/爭取疫苗代工!陳時中證實:正與莫德納藥廠洽談中